Mô hình VSEPR
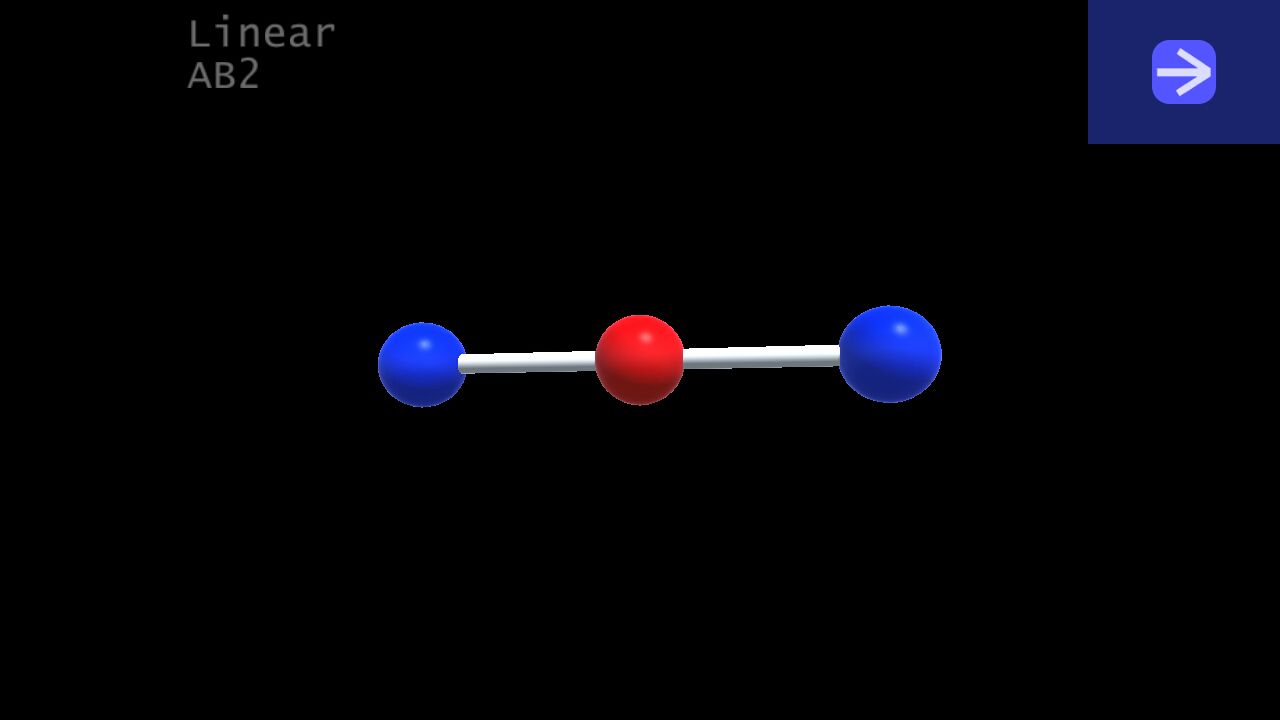
1. Linear (thẳng):
VSEPR Notation: AB2
Number of lone pairs (cặp e độc thân) : 0
Ideal bond angles: 180
Example: CO2, BeH2, BeCl2, HCN, N2O, C2H2
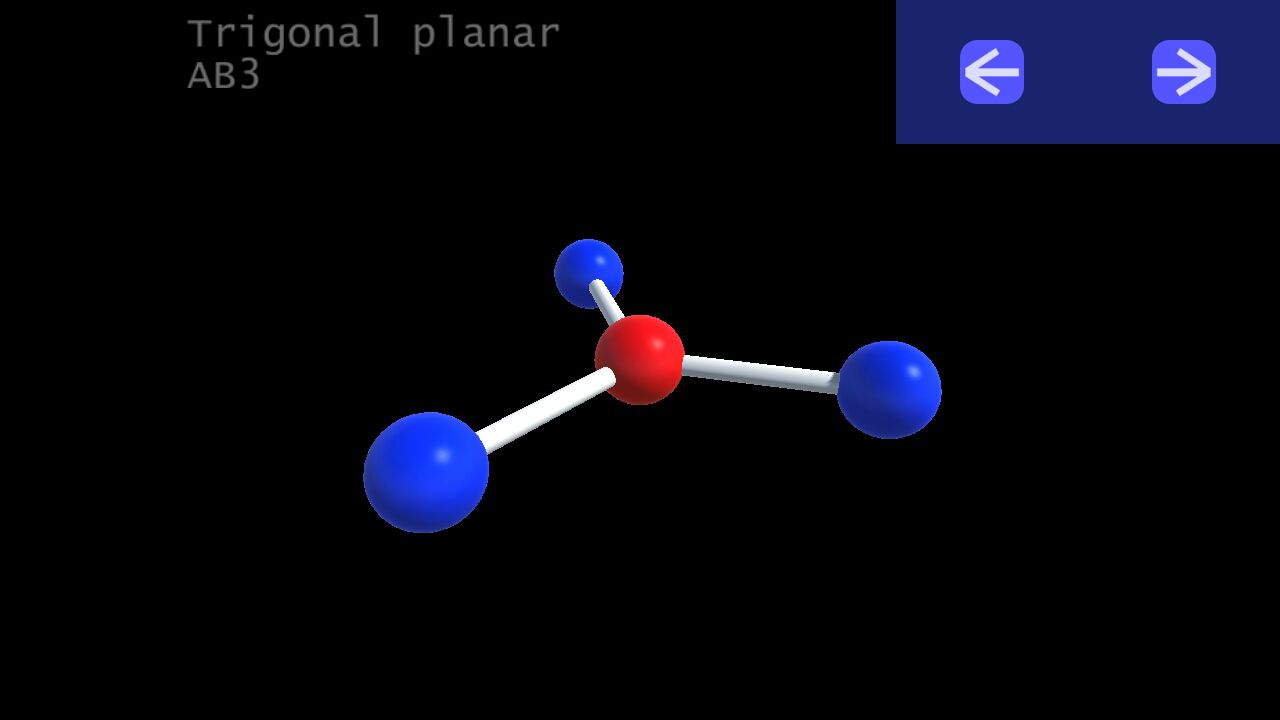
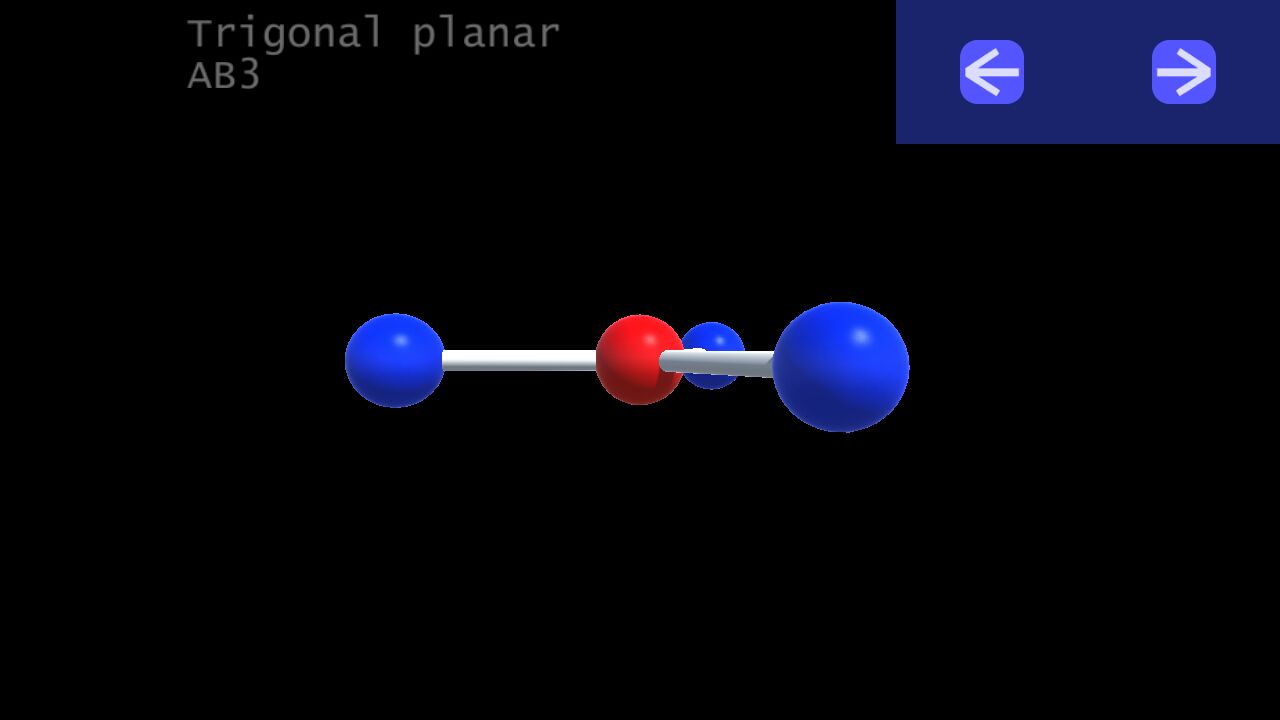
2. Trigonal planar (tam giác) :
VSEPR Notation: AB3
Number of lone pairs (cặp e độc thân) : 0
Ideal bond angles: 120
Example: BF3, HCHO, SO3, CO3(2-), NO3(-)
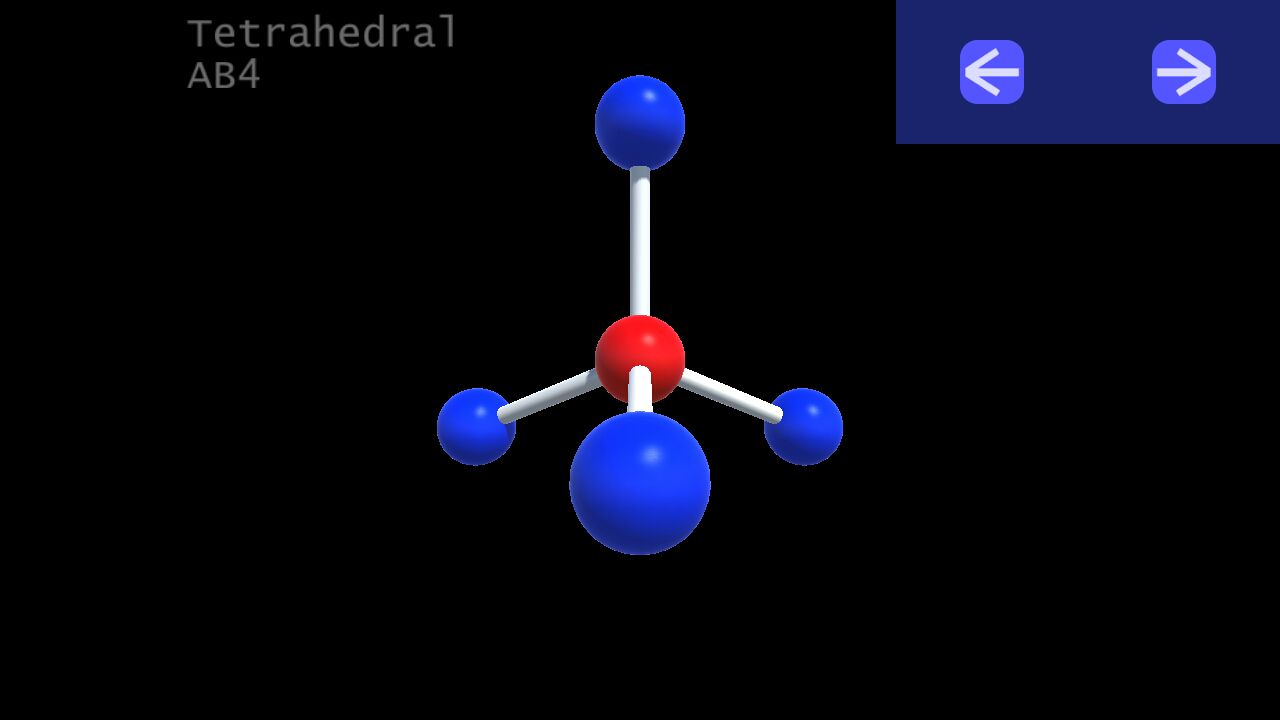
3. Tetrahedral (tứ diện):
VSEPR Notation: AB4
Number of lone pairs (cặp e độc thân) : 0
Ideal bond angles: 109,5
Example: CH4, SiCl4, NH4(+), SO2Cl2, SO4(2-), ClO4(-)
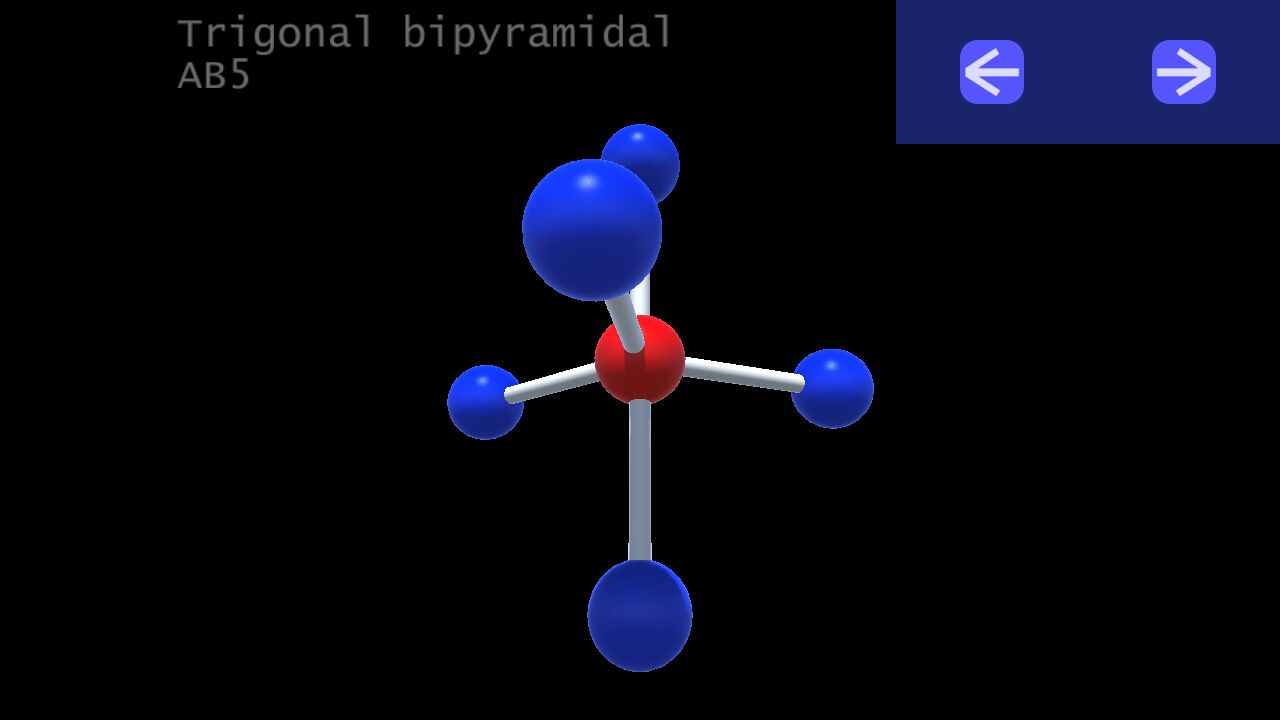
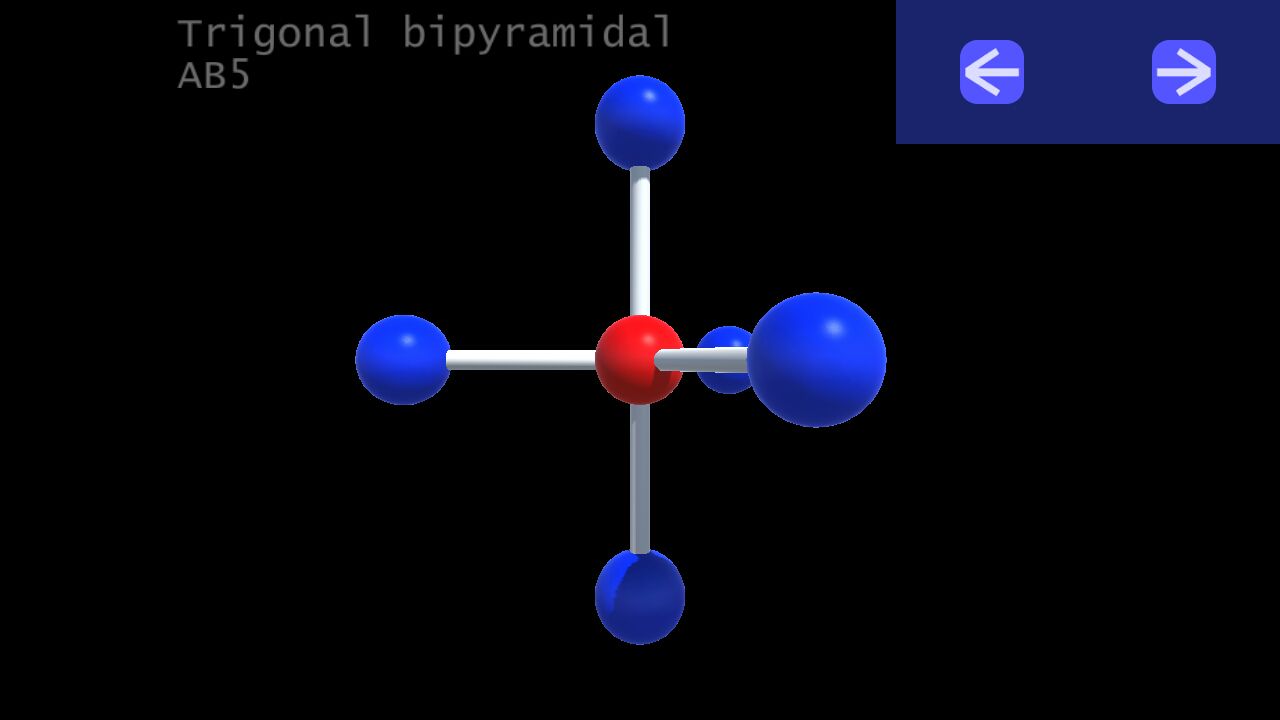
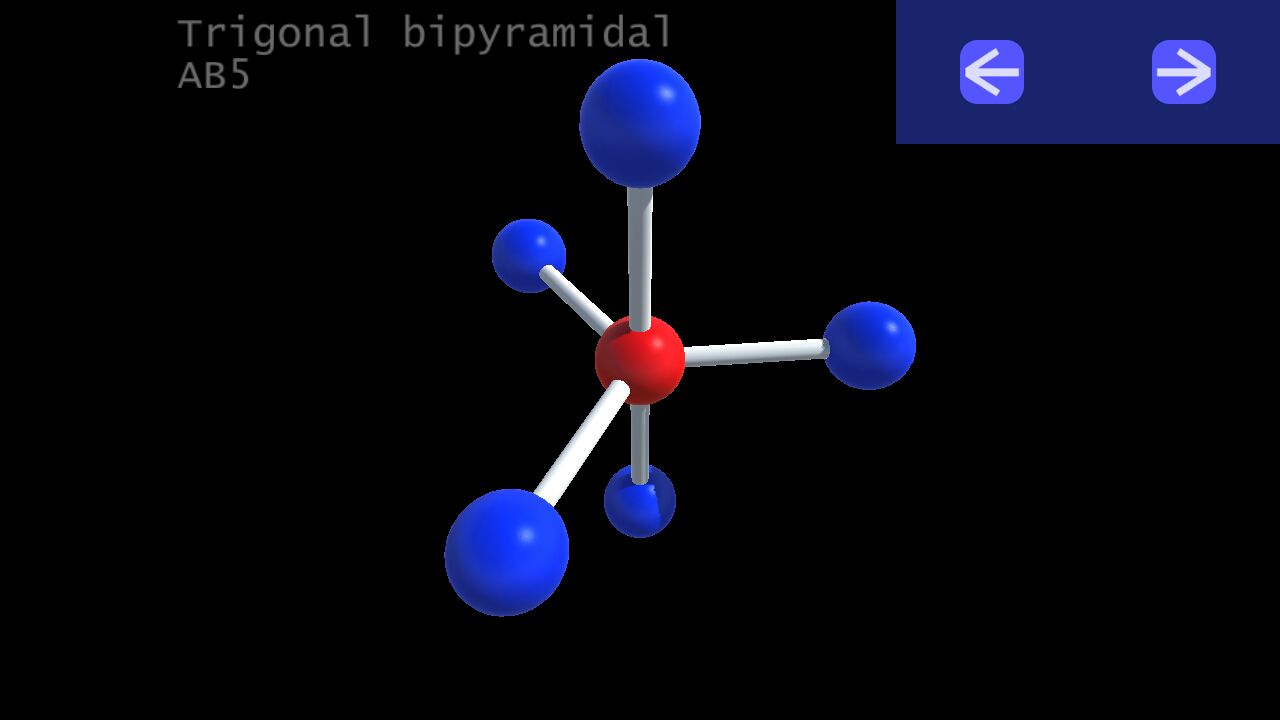
4. Trigonal bipyramidal (lưỡng tháp tam giác):
VSEPR Notation: AB5
Number of lone pairs (cặp e độc thân) : 0
Ideal bond angles: 90, 120
Example: PCl5, SOF4
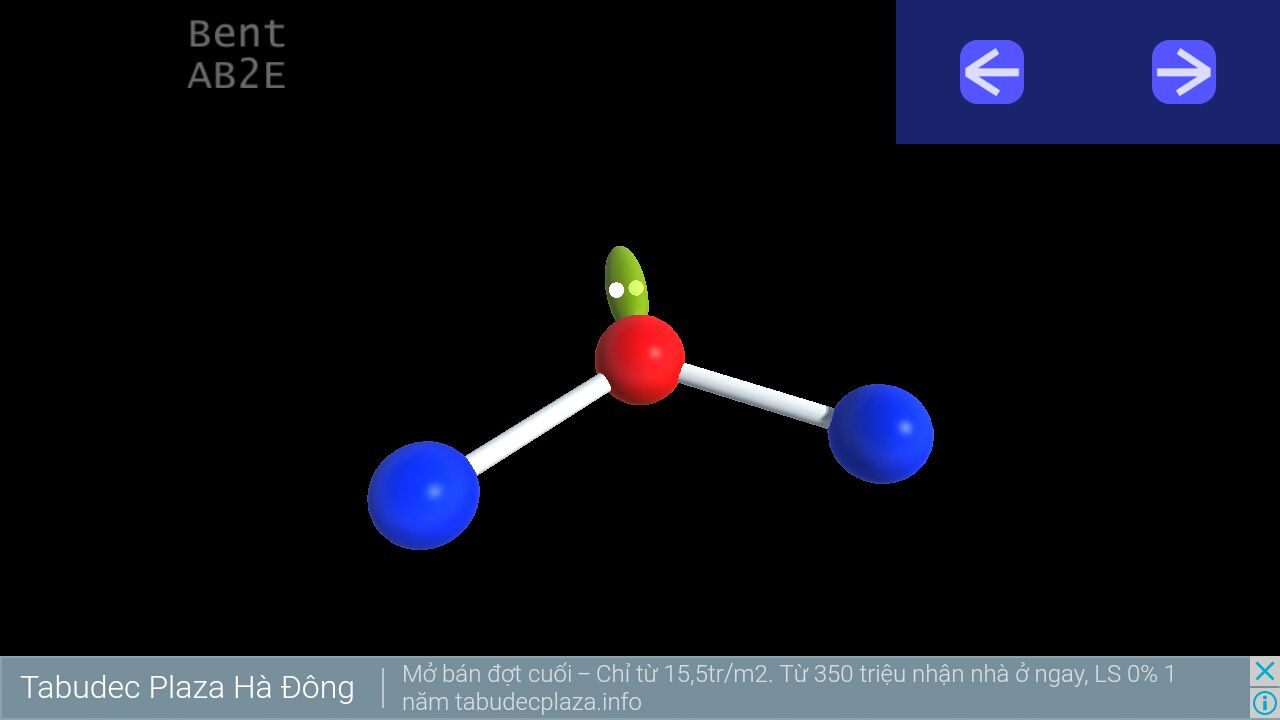
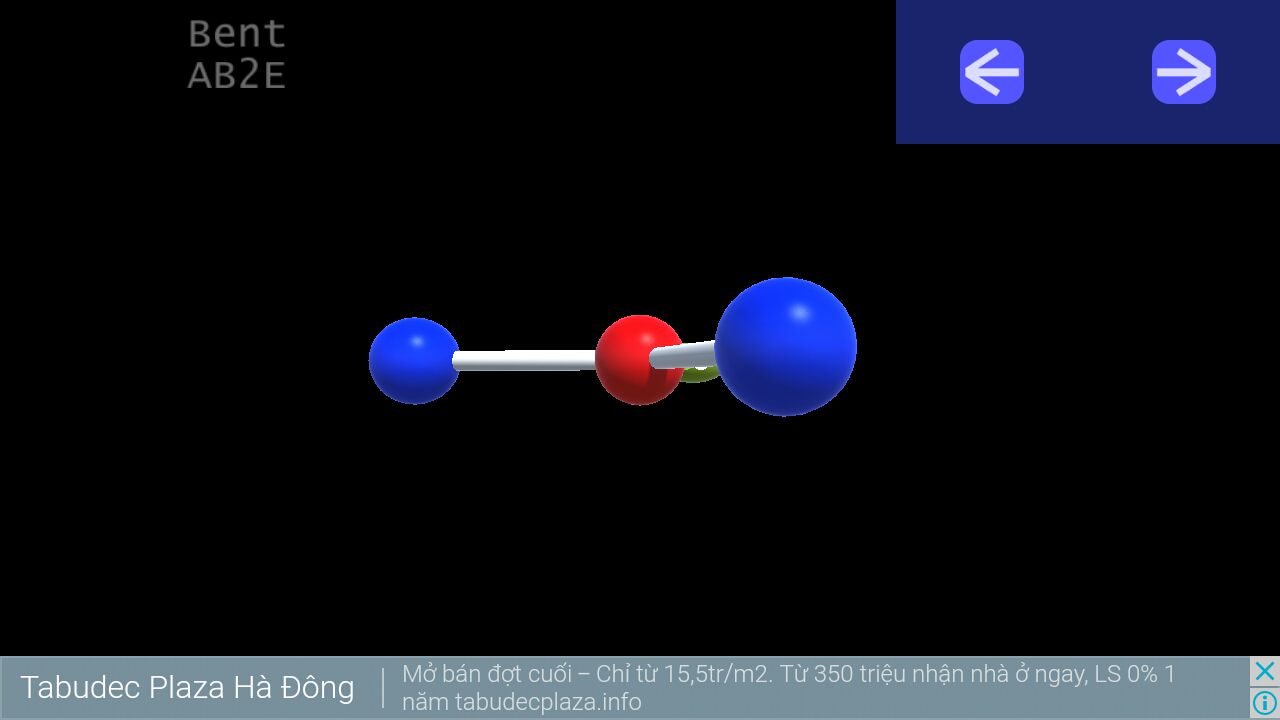
5. Bent (chữ V):
VSEPR Notation: AB2E
Number of lone pairs (cặp e độc thân) : 1
Ideal bond angles: 120
Example: SO2, O3, NO2, SnCl2
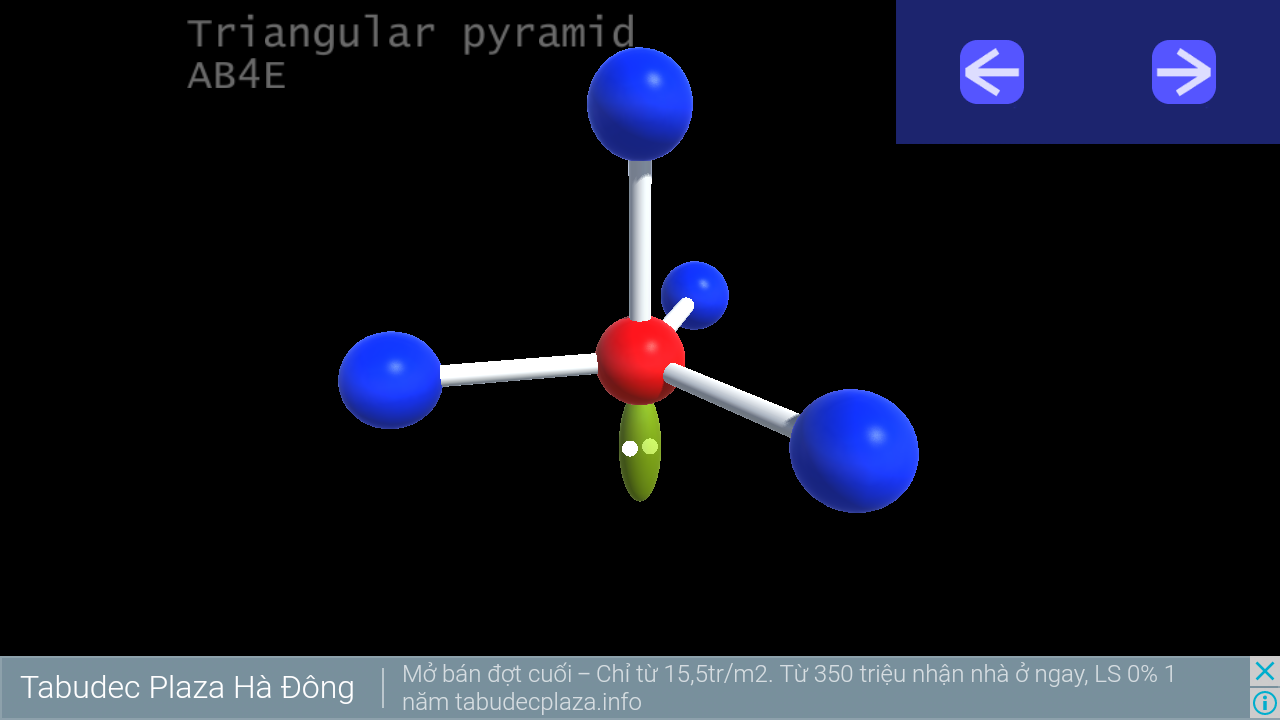
6. Trigonal pyramidal
VSEPR Notation:
Number of lone pairs (cặp e độc thân) :
Ideal bond angles:
Example:
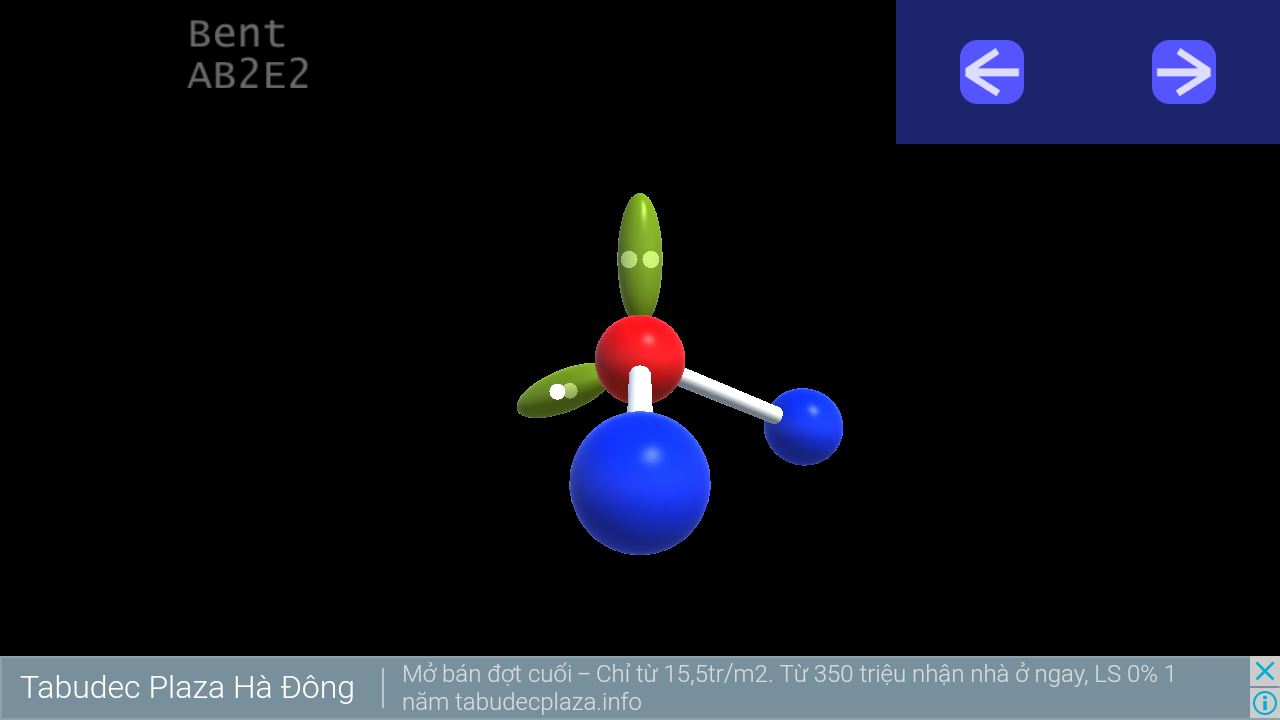
7. Bent
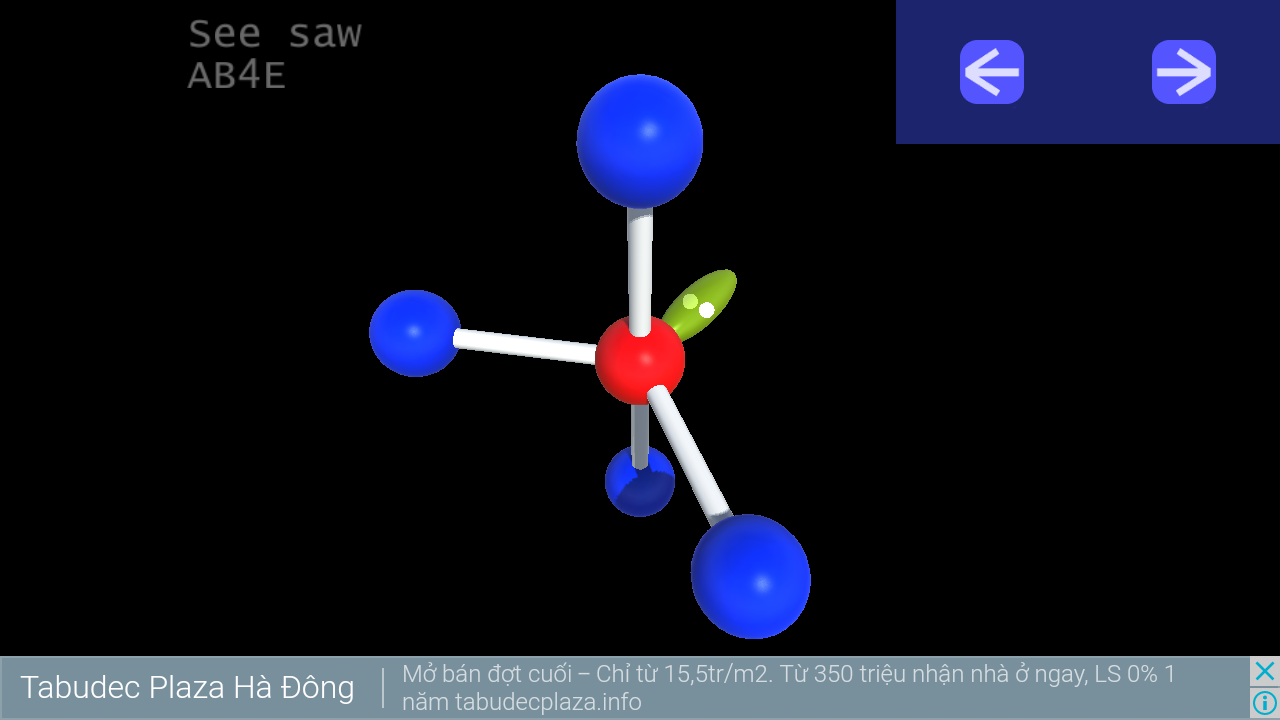
8. See saw
9. T-shape
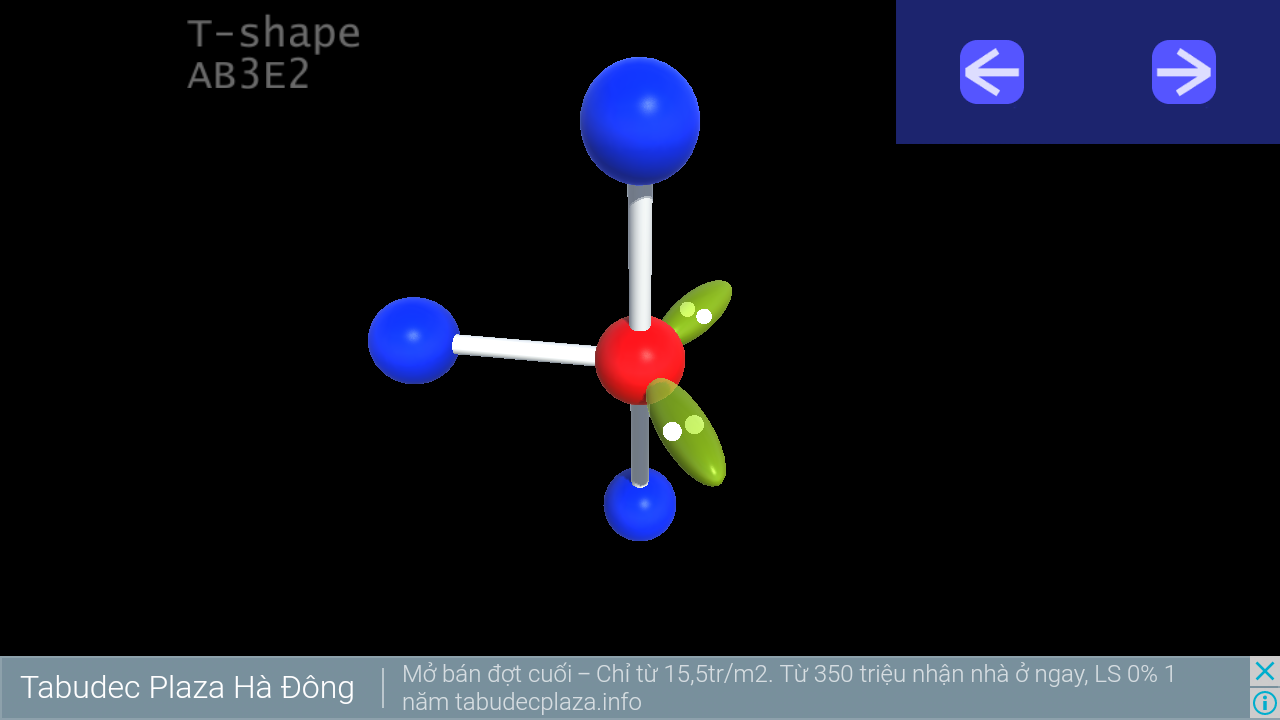
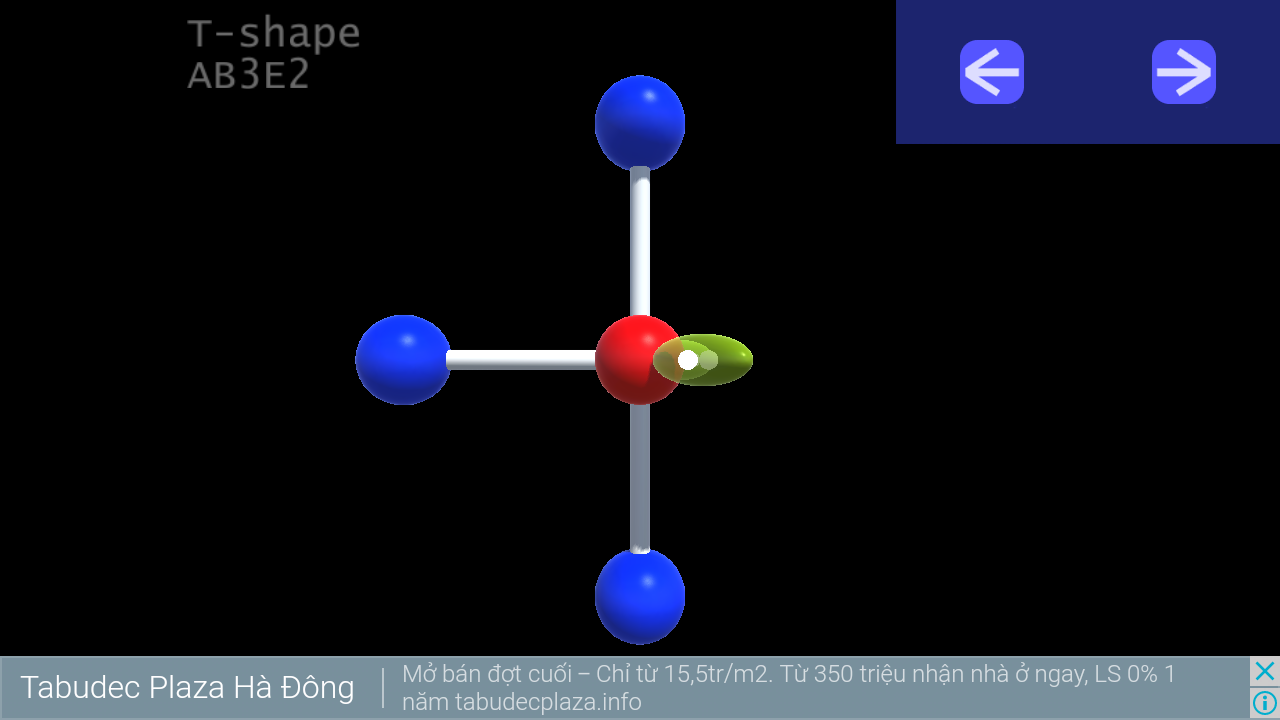
10. Triangular pyramid
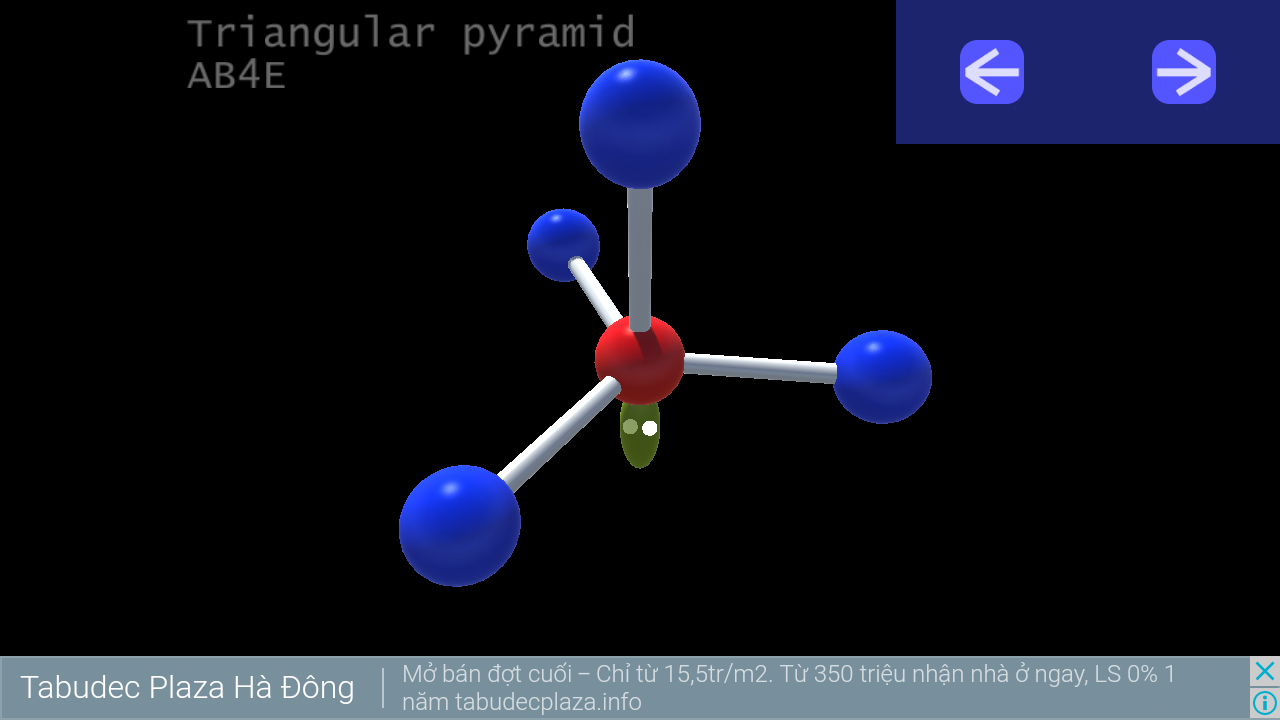
Bạn đang đọc truyện trên: Truyen4U.Com